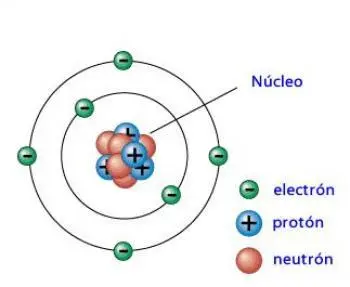
Un neutron est une particule subatomique qui fait partie de l'atome. Les atomes sont composés de protons, de neutrons et d'électrons. Les neutrons et les protons constituent le noyau atomique et sont également appelés nucléons. Selon le modèle atomique actuel, les électrons gravitent autour du noyau.
Le nombre atomique est le nombre de protons. Le nombre de masse est le nombre de protons et de neutrons dans le noyau. Le nombre différent de neutrons dans le noyau n'implique pas la variation de l'atome lui-même. Cependant, il détermine l'isotope auquel il fait partie.
Au départ, on croyait qu'il s'agissait d'une particule élémentaire, mais plus tard, on a découvert qu'elle était composée de quarks. Plus précisément, il comprend trois quarks, un up et deux down.
Le neutron est une particule de spin 1/2 ; c'est un fermion. Cependant, pendant de nombreuses années après la découverte du neutron, son tour exact était ambigu. Bien qu'il ait été supposé être une particule de Dirac de spin 1/2, la possibilité que le neutron soit une particule de spin 3/2 persistait.
Quelle est la durée de vie d'un neutron ?
La demi-vie d'un neutron à l'extérieur du noyau n'est que d'environ 885 secondes (15 minutes).
Quelle est la masse du neutron ?
La masse d'un neutron est de 1,67492729 × 10-27 kg.
Sa masse ne peut pas être déterminée directement par spectrométrie de masse en raison de l'absence de charge électrique. Cependant, elle peut être déduite en mesurant les masses d'un proton et d'un deutéron. Un deutéron est le noyau de deutérium, un isotope de l'hydrogène de numéro atomique 1 (un proton).
La masse de cette particule est légèrement supérieure à celle du proton.
Quelle est la charge du neutron?
La charge électrique totale du neutron est de 0 coulombe.
La limite pratique obtenue est si proche de zéro que le neutron est considéré comme n'ayant aucune charge par rapport à la charge du proton.
En revanche, les protons et les électrons, les deux autres sous-particules de l'atome, sont chargés. Ils ont la même charge électrique mais avec des signes différents. Par conséquent, un atome neutre a la même quantité de protons et d'électrons.
Qui a découvert le neutron ?
James Chadwick, physicien britannique et lauréat du prix Nobel, a découvert le neutron en 1932.
Quand Ernest Rutherford a soulevé son modèle atomique, il a donné une conférence à la Royal Society en 1920. Dans ce document, il a fait valoir qu'il doit y avoir une autre particule sans charge électrique dans le noyau de l'atome pour maintenir les protons ensemble.
La première indication de l'existence de cette nouvelle particule a eu lieu en 1930. Walther Wilhelm Georg Bothe et H. Becker ont découvert que le bombardement du béryllium avec des particules alpha produisait un rayonnement pénétrant. Initialement, ce rayonnement était considéré comme un type de rayonnement gamma.
En 1932, James Chadwick a proposé une explication alternative pour les particules non chargées à peu près de la même taille qu'un proton.
Cette nouvelle particule a été appelée un neutron en raison de sa charge électrique neutre.
Quelle est leur importance pour la fission nucléaire ?
Les neutrons sont un élément essentiel pour générer des réactions en chaîne dans un réacteur nucléaire. Les centrales nucléaires obtiennent de l'énergie grâce à des réactions de fission nucléaire.
Une réaction nucléaire de fission se produit lorsqu'un neutron frappe le noyau d'un atome d'uranium. Les atomes d'uranium enrichi sont instables et l'impact suffit à les briser. Deux ou trois autres neutrons libres sont générés dans chaque réaction qui peuvent entrer en collision avec d'autres atomes de combustible.
Dans l'énergie nucléaire, le concept « enrichissement d'uranium » fait référence à l'altération du nombre de neutrons dans le noyau atomique afin d'obtenir un autre atome d'uranium plus instable. Cette modification implique donc un changement isotopique.


