
L'uranium, élément chimique de grande importance dans le monde de la science et de la technologie, occupe une place de choix dans le tableau périodique en raison de ses propriétés uniques. Son numéro atomique est 92 et on le trouve dans la nature sous diverses formes.
L'uranium est surtout connu pour son rôle dans la production d'énergie nucléaire et la fabrication d'armes nucléaires, car il constitue l'élément clé de la fission nucléaire. De plus, il a des applications en médecine, dans la recherche scientifique et dans la technologie aérospatiale.
Bien que son utilisation présente des avantages significatifs, l'uranium est radioactif et sa manipulation est soumise à des réglementations strictes pour garantir son utilisation en toute sécurité.
Utilisations et applications
 L'uranium a plusieurs applications dans l'industrie et la recherche. Regardons quelques exemples :
L'uranium a plusieurs applications dans l'industrie et la recherche. Regardons quelques exemples :
- Production d'énergie nucléaire : L'uranium est principalement utilisé comme combustible dans les réacteurs nucléaires pour la production d'énergie électrique. L'uranium enrichi est utilisé dans la fission nucléaire, où les noyaux d'uranium 235 se divisent en noyaux plus petits, libérant une grande quantité d'énergie sous forme de chaleur. Cette énergie est convertie en électricité. L'énergie nucléaire est une source d'énergie propre et efficace.
- Fabrication d'armes nucléaires : L'uranium enrichi a également été utilisé dans la fabrication d'armes nucléaires. Lorsqu’une concentration suffisante d’uranium 235 est atteinte, il peut être utilisé pour créer des explosions nucléaires dévastatrices. Cela a conduit à la nécessité de contrôler et de restreindre l’accès à l’uranium enrichi.
- Médecine nucléaire : L'uranium est utilisé en médecine nucléaire dans la production de radio-isotopes, tels que le technétium-99m, qui sont utilisés en imagerie médicale, comme la tomographie par émission de positons (TEP) et la scintigraphie, pour le diagnostic de maladies et de troubles.
- Propulsion spatiale : la fission nucléaire de l'uranium est considérée comme une source d'énergie pour les missions spatiales de longue durée. La possibilité d'utiliser des réacteurs nucléaires pour propulser des engins spatiaux a été explorée.
- Recherche scientifique : L'uranium est utilisé dans la recherche scientifique, notamment dans les expériences nucléaires et les études sur la physique des particules. Il est également utilisé dans les accélérateurs de particules et les détecteurs de rayonnement.
- Projectiles perforants et perforants : L'uranium appauvri a été utilisé dans les projectiles perforants et le blindage des véhicules militaires en raison de sa haute densité, qui lui confère des propriétés pénétrantes et protectrices.
Structure d'un atome d'uranium
 Un atome est constitué d'un noyau et d'électrons qui entourent ce noyau. À son tour, un noyau est constitué de protons et de neutrons. Un proton a une charge positive. Un neutron n'a pas de charge électrique et est neutre.
Un atome est constitué d'un noyau et d'électrons qui entourent ce noyau. À son tour, un noyau est constitué de protons et de neutrons. Un proton a une charge positive. Un neutron n'a pas de charge électrique et est neutre.
Les charges positives des protons tentent de se repousser violemment. Ce qui les empêche de se séparer, c’est un nouveau type de force : une force d’attraction à courte portée, extrêmement puissante, qui agit de manière égale entre les protons et les neutrons (qui, de ce point de vue, sont tous des nucléons).
La force nucléaire à courte portée les maintient ensemble, s'opposant à l'effet répulsif des charges positives des protons. Les neutrons agissent ainsi comme un « ciment nucléaire ».
Types d'uranium : naturel, enrichi et appauvri
Il existe différents types d'uranium selon sa composition isotopique. Chacun de ces types possède des propriétés et des applications spécifiques, ce qui en fait des composants essentiels de la technologie nucléaire et d'autres disciplines connexes.
Vous trouverez ci-dessous une brève description de chaque type d’uranium et de leurs caractéristiques respectives.
uranium naturel
L'uranium naturel est celui que l'on trouve dans la nature et est principalement composé de trois isotopes : l'uranium-238 (U-238), l'uranium-235 (U-235) et l'uranium-234 (U-234). La proportion d’U-238 dans l’uranium naturel est bien supérieure à celle de l’U-235 et doit être enrichi pour être utilisé dans des réacteurs nucléaires ou des armes nucléaires.
Uranium enrichi
 L'uranium enrichi est un uranium dans lequel la proportion d'U-235 est augmentée par rapport à l'uranium naturel. Ce processus est réalisé dans des usines d'enrichissement et permet d'obtenir de l'uranium avec une concentration plus élevée en U-235. L'uranium enrichi est nécessaire pour alimenter la plupart des réacteurs nucléaires utilisés pour la production d'électricité.
L'uranium enrichi est un uranium dans lequel la proportion d'U-235 est augmentée par rapport à l'uranium naturel. Ce processus est réalisé dans des usines d'enrichissement et permet d'obtenir de l'uranium avec une concentration plus élevée en U-235. L'uranium enrichi est nécessaire pour alimenter la plupart des réacteurs nucléaires utilisés pour la production d'électricité.
Uranium appauvri
L'uranium appauvri est de l'uranium qui a subi un processus d'enrichissement pour augmenter la concentration en U-235, et le matériau restant, qui a une concentration plus faible en U-235, est connu sous le nom d'uranium appauvri. Ce matériau a des utilisations limitées et est souvent stocké ou utilisé dans des applications non nucléaires.
L'uranium dans le tableau périodique
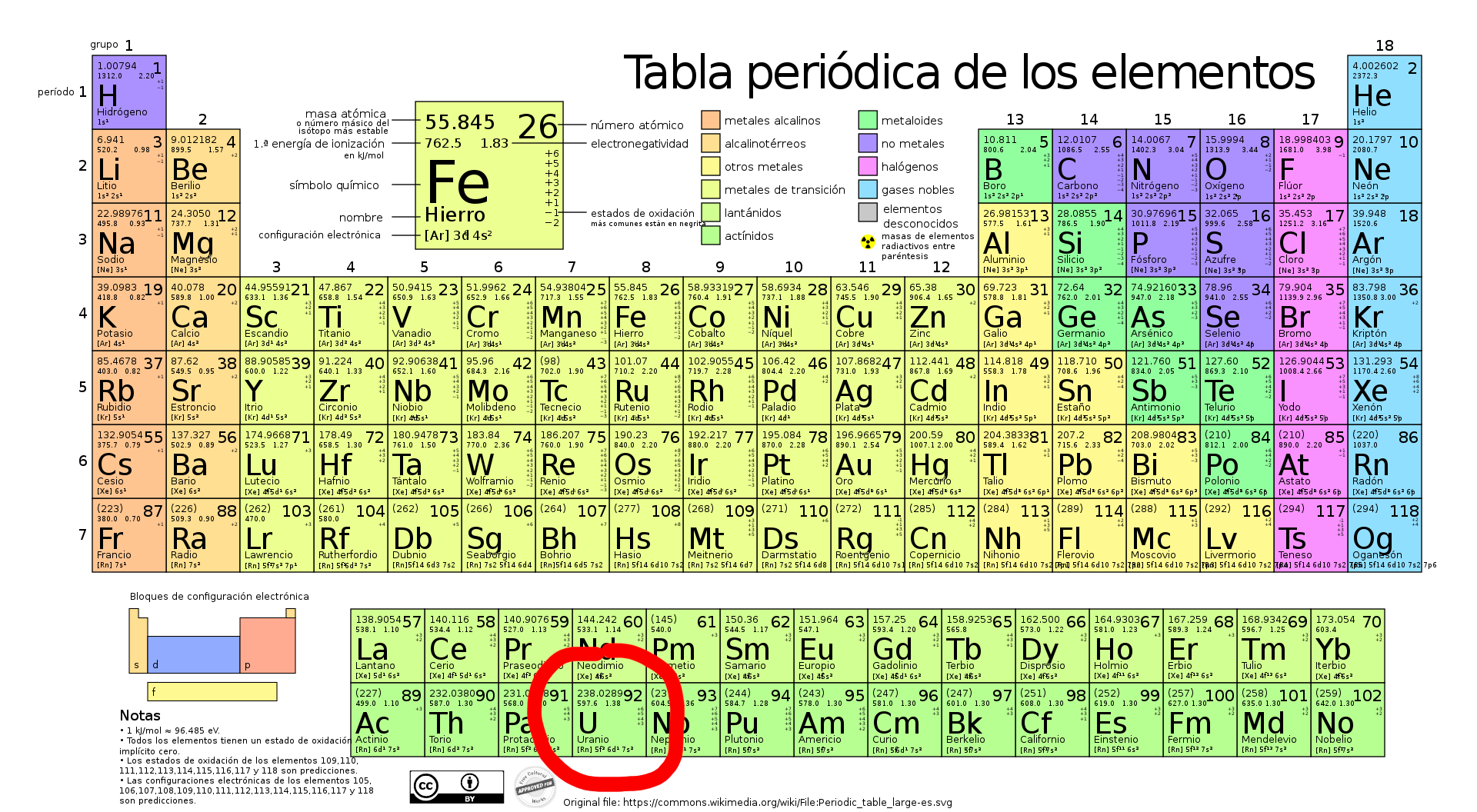
L'uranium, avec le symbole « U » et le numéro atomique 92 sur le tableau périodique, est un élément radioactif contenant plusieurs isotopes notables trouvés dans le groupe 3 du tableau périodique.
Il appartient à la période 7, ce qui signifie que son septième niveau d'énergie contient des électrons. Concernant son bloc, il est classé comme élément du bloc f, spécifiquement dans la série des actinides.
Cet élément fait partie de la série des actinides en raison de la similitude des propriétés électroniques des éléments de ce groupe.
|
Propriété |
Valeur |
|
symbole chimique |
OU |
|
Numéro atomique |
92 |
|
Masse atomique (U-238) |
Environ 238.05078 u |
|
État physique |
Solide à température ambiante) |
|
Isotopes importants |
U-238, U-235 |
|
Point de fusion |
Environ 1 132 °C (2 070 °F) |
|
Point d'ébullition |
Environ 3 818 °C (6 904 °F) |
|
Propriétés radioactives |
Émet des rayonnements alpha, bêta et gamma |
|
Toxicité |
Toxique pour les humains |
|
Applications |
Énergie nucléaire, armes nucléaires, datation radiométrique |
|
Abondance |
Relativement rare, on le trouve dans des minéraux comme l'uraninite et la carnotite. |
Isotopes de l'uranium
L'uranium peut être présent dans différentes compositions dans son noyau, c'est-à-dire dans différents isotopes. Bien que l’uranium puisse être trouvé dans la nature, sa majeure partie se trouve dans une configuration qui n’est pas la plus adaptée pour générer des réactions nucléaires.
Pour cette raison, les atomes de cet élément sont artificiellement modifiés pour les convertir en d’autres isotopes plus instables. Ces nouveaux isotopes favoriseront la génération de réactions en chaîne de fission nucléaire.
Voici les isotopes les plus importants :
-
Uranium 235 (U-235) : C'est l'isotope de l'uranium utilisé comme combustible dans les réacteurs nucléaires et pour la fabrication d'armes nucléaires. L'U-235 est fissile, ce qui signifie qu'il peut se diviser en deux noyaux plus légers lorsqu'il absorbe un neutron, libérant ainsi une grande quantité d'énergie sous forme de chaleur et de rayonnement. Ce processus est fondamental dans les réactions de fission nucléaire et constitue le principe derrière les bombes nucléaires et la production d'électricité dans les réacteurs nucléaires.
-
Uranium 238 (U-238) : C'est l'isotope de l'uranium le plus abondant et constitue la majeure partie de l'uranium naturel. L'U-238 peut également fission, mais n'est pas fissible par les neutrons thermiques, ce qui le rend moins utile pour la plupart des applications de fission nucléaire. Cependant, l'U-238 est converti en plutonium-239 (Pu-239) lorsqu'il absorbe un neutron, et le Pu-239 est une autre matière fissile utilisée dans la fabrication d'armes nucléaires et comme combustible dans les réacteurs à fission.
-
Uranium-233 (U-233) : Bien que moins courant, l'U-233 est un autre isotope fissile de l'uranium qui peut être utilisé comme combustible dans les réacteurs nucléaires. Il est formé à partir du thorium 232 (Th-232) par absorption d'un neutron. Bien qu’il s’agisse d’un produit fissile efficace, il est plus compliqué à produire et à manipuler que l’U-235 ou le Pu-239.
En plus des isotopes mentionnés, il existe d’autres isotopes moins courants. Il s'agit notamment de l'uranium 234 (U-234), de l'uranium 236 (U-236), de l'uranium 239 (U-239), entre autres. Ces isotopes sont moins abondants et ont des applications plus limitées en technologie nucléaire en raison de leur faible prévalence.


