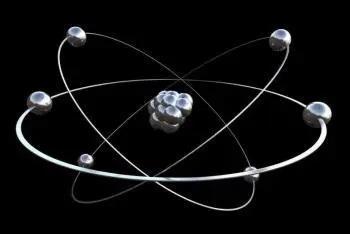
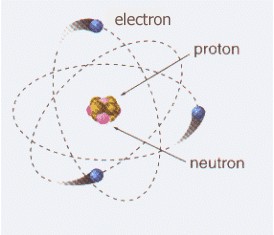
Un électron est une particule élémentaire stable chargée négativement. Avec les neutrons et les protons, c'est l'une des trois sous-particules qui composent un atome. Pour cette raison, elle peut également être définie comme une particule subatomique. Il fait partie du groupe des leptons.
Ils peuvent apparaître à l’état libre (sans être liés à aucun atome) ou liés au noyau d’un atome.
Le piège Penning est souvent utilisé pour mesurer ce type de particules .
Les électrons existent dans les atomes dans des coques sphériques de différents rayons. Ces coques sphériques représentent les niveaux d'énergie. Plus la coque sphérique est grande, plus l'énergie contenue dans cette particule élémentaire est grande.
Énergie électrique
Dans les conducteurs électriques, les flux de courant sont les électrons des atomes qui circulent individuellement d’un atome à l’autre dans le sens allant du pôle négatif au pôle positif du conducteur électrique. C'est ce que nous appelons l'énergie électrique ou l'électricité.
Bien qu’ils fassent généralement partie des atomes, certains électrons forment des faisceaux dans le vide ou se déplacent indépendamment dans la matière.
 Dans les matériaux semi-conducteurs, le courant électrique est également produit par le mouvement de ces sous-particules.
Dans les matériaux semi-conducteurs, le courant électrique est également produit par le mouvement de ces sous-particules.
Charge électrique de l'électron
La charge d'un électron est d'environ -1,602 x 10-19 coulombs (C).
L'unité de charge électrique élémentaire est la charge électrique d'un électron. Cette charge élémentaire est la plus petite charge trouvée dans la nature et est considérée comme une quantité fondamentale en physique des particules et en théorie électromagnétique.
La charge électrique de l’électron est considérée comme négative en raison de conventions historiques et la charge des protons (qui est positive) a été définie en fonction de la charge des électrons. Ce choix de signes a été largement accepté en physique et en électronique.
La charge d’un proton, qui est une autre sous-particule élémentaire, est égale en ampleur mais de signe opposé à la charge de l’électron.
Expérience de goutte d'huile Millikan
Le but de l'expérience de Robert Millikan et Harvey Fletcher sur les gouttes d'huile était de déterminer la charge d'un seul électron. Pour ce faire, ils ont maintenu une petite goutte d’huile flottant entre deux plaques du condenseur.
Ils ont découvert que les valeurs mesurées étaient toujours des multiples d’une même charge. Ils ont interprété cela comme une charge sur un seul électron : 1,602 × 10−19 Coulomb.
En 1923, Millikan remporta le prix Nobel de physique.
Masse électronique
Sa masse est d'environ 9,11 x 10-31 kg.
Les électrons qui se déplacent à une fraction appréciable de la vitesse de la lumière ont une masse plus grande en raison des effets relativistes. Autrement dit, la masse de l’électron augmente avec la vitesse, conformément aux prédictions d’Albert Einstein.
Importance des électrons
Ces particules subatomiques fondamentales jouent un rôle essentiel dans divers aspects de la physique, de la chimie et de la technologie.
Son importance réside dans plusieurs aspects :
Électricité et courant électrique
Les électrons portent une charge électrique négative et sont responsables de l’électricité et du courant électrique. Le courant électrique est essentiel dans presque tous les aspects de notre vie quotidienne, de l’éclairage à l’électronique et à la production d’électricité.
Matériaux conducteurs
 Les matériaux conducteurs permettent aux électrons de se déplacer librement à travers eux. Ceci est crucial dans la fabrication de câbles électriques, de composants et de circuits électroniques, facilitant la transmission de l’énergie et des signaux électriques.
Les matériaux conducteurs permettent aux électrons de se déplacer librement à travers eux. Ceci est crucial dans la fabrication de câbles électriques, de composants et de circuits électroniques, facilitant la transmission de l’énergie et des signaux électriques.
Liens chimiques
En chimie, ces particules participent à la formation de liaisons chimiques entre atomes. Le partage et le transfert d’électrons entre atomes permettent la formation de molécules et de composés chimiques, ce qui est fondamental pour la chimie et la vie elle-même.
Propriétés matérielles
Les électrons déterminent de nombreuses propriétés des matériaux, telles que leur conductivité électrique, leur conductivité thermique et leurs propriétés magnétiques. Ces propriétés sont essentielles dans la fabrication d’appareils électroniques, de matériaux magnétiques, etc.
Rayonnement et spectroscopie
En physique, les électrons sont impliqués dans des processus de rayonnement, tels que l’émission et l’absorption de la lumière. La spectroscopie, qui utilise l'interaction des électrons avec le rayonnement électromagnétique, permet d'analyser la composition des substances et de comprendre les phénomènes astronomiques.
Electronique et technologie
Les appareils électroniques, tels que les ordinateurs, les téléphones portables, les téléviseurs, etc., fonctionnent grâce à la manipulation d'électrons. Les progrès de l’électronique ont transformé la société et la technologie modernes.
Physique des particules
En physique des particules, les électrons sont des particules fondamentales étudiées dans les accélérateurs de particules. Comprendre leur comportement a conduit au développement de théories fondamentales sur la structure de la matière et les interactions fondamentales.
Histoire et découverte
La découverte de l'électron est principalement attribuée à JJ Thomson, physicien britannique, à la fin du XIXe siècle. En 1897, Thomson a mené des expériences en utilisant un tube cathodique, un dispositif impliquant du courant électrique et des décharges dans un vide partiel.
Thomson a observé qu'il y avait de minuscules particules avec une charge électrique négative se déplaçant de la cathode vers l'anode à l'intérieur du tube cathodique. Ces particules ont été appelées « électrons » par Thomson.
Ses expériences démontrèrent que les électrons étaient des constituants fondamentaux de la matière et qu'ils entretenaient une relation spécifique entre leur charge et leur masse, révélant leur existence en tant que particules subatomiques.
Le modèle atomique de Thomson est le premier modèle atomique dans lequel est mentionnée l'existence d'électrons dans la composition d'un atome.
Cette découverte était révolutionnaire et posait les bases d’une nouvelle compréhension de la structure atomique et des interactions électriques au niveau subatomique. En outre, cela a ouvert la voie à des développements ultérieurs en physique, en chimie et en technologie, notamment en électronique moderne et en théorie quantique.